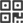迄今为止,EIT开发的Cellular Titanium植入物已经用在了来自15个国家的10000个病例中。FDA批准允许EIT首次在美国销售这种椎间融合器,这是EIT的一个重要里程碑。

Cellular Titanium是用选择性激光熔融(SLM)增材制造而成的,有80%的孔隙率,极大促进了骨修复所需的细胞生长。此外,如果研究发现了能优化孔隙率或植入物设计的新参数,SLM将允许EIT轻松重新设计设备并重新申请批准。
在此时进入美国市场,EIT面临着不小的竞争。前不久,弗吉尼亚医疗器械制造商K2M的可调节3D打印MOJAVE PL腰椎支撑融合器获得了FDA批准。2016年3月,Stryker的3D打印Tritanium腰椎融合器获得了FDA批准,并且已经在尝试用PEEK塑料来3D打印植入物。







 大家都在看
大家都在看




 3D打印直通车
3D打印直通车 上传STL文件
上传STL文件 挑选模型
挑选模型