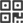近年来,3D打印医疗器械技术及应用成为业界热议的话题,不少企业亦花费巨资研发新技术与产品。3D打印医疗器械产品有节省资源、实现定制化等诸多优点,但目前而言,该技术仍然存在相关产品风险凸显等众多问题,而其背后则是国内3D打印医疗器械相关标准没有建立的尴尬处境。所以,国内很多医院对于3D打印技术的投入使用一直处于保守。

高端设备成“看病贵”主因3D打印器械法规不健全
所谓工欲善其事必先利其器,医院的硬件设施特别是诊治仪器的质量,关乎最终医疗结果。目前全球的高端医疗设备制造商依然以德国、美国、日本为主,甚至达到了垄断的地位。因为众多医院出于保证医疗水平的目的,不惜花费重金引入进口设备用于临床诊治。设备大到核磁共振MRI、电脑断层CT、手术机器人等,小到手术剪刀、镊子、夹子等(如德国蛇牌血管钳持针器镊子,仅一个就售价300欧,折合人民币约2400元)。
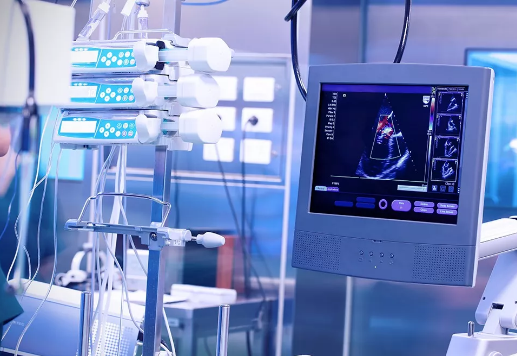
在10月9日举行的2018年中国医院创新发展峰会暨北京大学第三医院建院60周年学术研讨会上,北医三院大外科主任、骨科专家刘忠军透露:“看病贵,医疗器械贵是个大原因,在骨科手术中,器材的费用要占到整个医疗费用的三分之二。涉及到脊柱外科,国内三甲医院基本使用的都是进口器材。
刘忠军正在展示3D打印的骨骼
对于解决“看病贵”的问题,刘忠军表示通过3D打印技术有助于解决,“在3D金属打印技术刚刚问世时,我们就抓住时机,一直处于世界领先位置。但目前国内3D打印医疗器械仍面临相关标准没有建立等尴尬问题。例如很多3D打印器材需要根据不同病人的具体症状进行专门化定制,但我国目前还缺乏相关法规。”刘忠军说,“当一个病例没有更好的救治办法时,能使用3D打印是一件好事,但一旦出了问题,没有相关法规来保护医生的权益。”他透露,目前国家有关部门正在制定3D打印等医疗器械定制化法规,未来还会组织成立专家委员会,以帮助参评、审批后续的3D打印器械。
美国定制器械监管模式近百个3D打印器械已获批准
在美国,定制类器械(CustomizedDevice)泛指具有“个性化设计”和“定制式生产”特点的医疗器械。定制类器械可包括定制器械(CustomDevice)和患者匹配器械(Patient-matchedDeviceorPatient-specificDevice)两种类型,FDA(美国食品药品监督管理局)分别采用不同的模式进行管理。其中,患者匹配器械遵循常规医疗器械的监管模式,而定制器械则根据特定要求,采用简化的监管模式。

根据FDA公布信息,目前已批准的患者匹配器械主要包括骨科手术导板、骨科关节置换假体、颞下颌关节假体、齿科基桩等。这些产品均获得510(k)批准上市,通过与参照器械进行比较,证明申报产品与已上市产品实质性等同。其中,参照器械可以是以上市的其他患者匹配器械,也可以是规格尺寸定型的常规器械;既可以是通过传统工艺生产的医疗器械,也可以是用新工艺(如3D打印)加工而成的产品。参比项目主要是产品的预期用途、适应证、设计和材料等,并不体现加工工艺。而3D打印技术无疑是实线定制器械或患者匹配器械的一个重要助力。
需要注意的是,FDA并没有为3D打印器械另行制定相应的监管要求,仍需通过510(k)或PMA批准上市。究其原因,FDA风险分类的依据是产品预期用途,而非产品生产加工方式。根据FDA目前公布的信息,已有近百个3D打印医疗器械产品获得批准,包括气管夹板、颅骨板、髋关节假体、脊柱椎间融合器和齿科/骨科重建产品,均为第Ⅱ类医疗器械,通过510(k)申请上市,目前尚无PMA批准的3D打印器械。
注:为了在美国上市医疗器械,制造商必须经过两个评估过程其中之一:上市前通知书[510(k)](如果没有被510(k)赦免),或者上市前批准(PMA)。大多数在美国进行商业分销的医疗器械都是通过上市前通知书[510(k)]的形式得到批准的。在某些情况下,在1976年5月28日之前合法上市的器械,既不要求递交510(k)也不要求递交PMA。
而前述常规医疗器械、患者匹配器械都可以通过3D打印加工获得。对于定制器械,虽然FDA没有公开批准产品的相关信息,但定制器械的定义中明确了生产加工方式不限,说明定制器械可以通过3D打印方式生产加工。综上,由于采用不同的生产工艺并不会直接影响产品风险分类和监管模式。
国内3D打印医疗器械技术相关标准进行中
2015年全国两会期间,刘忠军院长就曾提出成立加快3D打印医疗科技创新产品审批和应用的建议。同年,该院设计研发的用于髋关节置换的3D打印髋臼杯被原国家食品药品监管总局批准注册上市,迄今已在国内应用上千例。
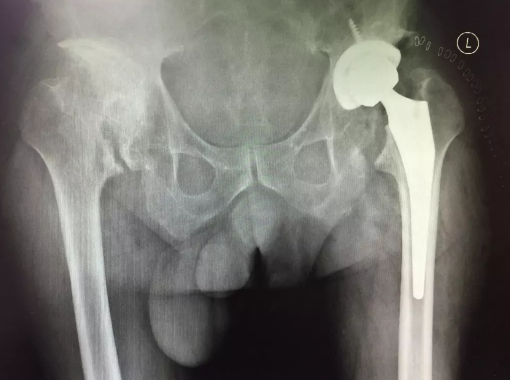
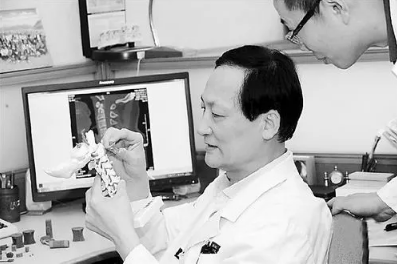
采用3D打印涂层的髋臼杯,具有坚强的骨质把持力,达到了完美的初始固定。
今年2月底,医疗器械技术审评中心公布了《定制式增材制造医疗器械注册技术审查指导原则》(征求意见稿),将国内3D打印医疗器械的临床应用和上市流通提上日程,3D打印与医疗器械行业迎来重大利好。
8月,中国食品药品检定研究所发布关于公开征求行业标准《用于增材制造的医用Ti-6Al-4V粉末》意见的通知。项目由国家药品监管局提出,中检院为归口单位,标准起草单位为北京爱康宜诚医疗器材有限公司及中检院等。据悉,医用増材制造Ti-6Al-4V粉末是3D打印钛合金植入物的原料,制定其标准旨在为医用粉末原料供应商、医疗器械制造商和监管部门等提供粉末特性评价和质量控制参考,为相关企业质量管理提供指导,也为监管部门制定相关法规政策提供技术支持。

目前,中检院初步建立了医用增材制造技术标准体系框架。由于现阶段缺乏相关评价技术,中检院承担了“十三五”科技部重点研发计划课题“3D打印医疗器械检验和评价技术研究”。基于前期的标准化研究,《用于增材制造的医用Ti-6Al4V粉末》(3D打印医疗器械用粉末的要求)和《3D打印钛合金植入物金属离子析出评价方法》两项标准将于2018年底完成报批。







 大家都在看
大家都在看




 3D打印直通车
3D打印直通车 上传STL文件
上传STL文件 挑选模型
挑选模型